
行业资讯
诺亚创生汇聚了行业内资讯内容,为您提供最新、最热的资讯内容。
外泌体通过独特机制修复子宫损伤,提高生育力
近日,Liu等人在《ACS Publicationgs》发表了一篇关于胎盘间充质干细胞(PMSCs)外泌体治疗子宫损伤的效果和分子机制研究,发现PMSCs外泌体通过miR-125b-5p、miR-30c-5p和miR-23a-3p调节TGF-β/smad通路,达到修复子宫内膜损伤并提高受损动物的生育能力。

子宫内膜损伤会导致宫腔粘连(IUA),主要继发于外伤、刮宫、感染、子宫先天畸形等因素,IUA的主要病理改变是子宫内膜纤维化和疤痕形成,因此抑制纤维化形成和促进疤痕愈合是IUA治疗的关键。
方法和目的:分别构建大鼠子宫损伤的体内模型和TGF-β1诱导的体外IUA模型,将大鼠随机分为正常组、IUA组和外泌体组。主要目的是验证外泌体对损伤子宫的保护作用以及抑制子宫内膜细胞纤维化背后的病理机制,并分析外泌体传递的特定miRNA是否有助于IUA靶向治疗(见下图)。
结果:①安全性分析:在治疗后第七天采集大鼠外周血,分析血细胞成分和血清生物化学,发现与正常组相比,使用外泌体进行宫内治疗不会导致大鼠血细胞计数或血细胞比容水平异常,生化指标均在正常范围内。
②生育能力分析:正常组的子宫样本,未经任何处理,均表现出受精后接受胚胎的能力;IUA组的左侧子宫的生育能力明显低于正常组;外泌体组治疗后左侧子宫的生育力增强(下图b)。此外,外泌体组的胚胎发育表现出与正常组相似(下图c)。
IUA组左侧子宫妊娠率为50%;外泌体组则飙升至83.33%(上图d)。外泌体组左侧子宫内的胚胎发育良好,其数量和大小均明显大于IUA组(上图e,f)。表明PMSCs外泌体促进了胚胎着床所需的功能性子宫内膜的再生,并促进其生育能力的恢复。
③子宫内膜厚度和腺体分析:使用HE染色评估子宫形态并测量子宫内膜厚度和腺体计数,正常组的平均子宫内膜厚度为552μm;IUA组的平均子宫内膜厚度降至193μm;外泌体组的厚度为427 μm,小于正常组,但明显大于IUA组(下图a,d)。

正常组腺体结构和数量均正常;IUA组的腺体数量显著减少;与IUA组相比,外泌体组的腺体比例较高,且结构相对完整(上图a,e)。这些发现表明,PMSCs外泌体可以增加受损子宫内膜的厚度和腺体数量。
④纤维化水平分析:Masson染色显示,外泌体组治疗14天后,纤维化水平显著降低(下图c,g);与正常组相比,IUA组纤维化相关蛋白的表达水平显著升高,经外泌体处理后相关蛋白水平显著改善(下图h,i)。表明PMSCs外泌体可有效减少子宫内膜纤维化程度。
⑤分子机制分析:关于这些治疗效果背后的分子机制,通过该研究确定了三种特定的miRNA,即miR-125b-5p、miR-30c-5p和miR-23a-3p,它们富含于PMSCs外泌体中,是治疗IUA的关键参与者。
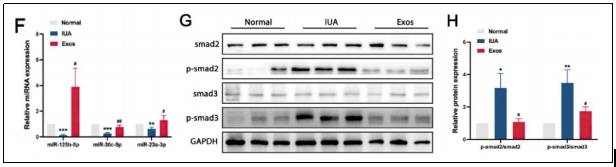
具体机制是miR-125b-5p、miR-30c-5p和miR-23a-3p通过靶向smad2和smad3的3'非翻译区来抑制smad2和smad3的表达,从而导致转化生长因子-β (TGF-β)/smad信号通路下调和纤维化的逆转(上图f,g,e)。
总 结:上述研究结果表明,PMSCs外泌体可有效促进IUA子宫内膜恢复,提高生育能力。此外,该研究还阐明了外泌体对IUA产生治疗作用的特定miRNA和潜在的分子机制,miRNA治疗靶点的确定,为IUA的精准治疗和利用外泌体的无细胞治疗提供了新的方向。

